刘强医生的科普号
- 媒体报道 乳腺癌成世界第一大肿瘤,一线城市女性终身患病率1/20
https://m.mp.oeeee.com/a/BAAFRD000020220418672929.html南方都市报,2022年4月19日35岁的年轻妈妈念念,在分娩后的四个月就被哺乳时候发现的肿块
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1240人已读 - 诊后必读 广东省惠民保最全合辑来啦!
https://mp.weixin.qq.com/s/dRBhANGcVr_lc5CBfj2yWw2021年末,2022年初,各地惠民保项目仍在加速落地,在市场分化,构建多层次医疗保障体系等的多重诉求之下,惠民保持续受到瞩目。惠民保是由政府指导的商业医疗保险,由医保局推动,多家保险公司作为一个共保体共同承保的。主要对标百万医疗险,打破百万医疗险无法惠及的老年人群、非标人群的现象,弥补医保不足,解决“住院医疗费用贵的问题”“因病返贫的问题”。广东省的惠民保时间最久,覆盖面最广,成为当之无愧的“惠民保高地”,提升了各大群体的医疗保障。目前,在广东省所有城市都已经陆续推出了惠民保,为了帮助患者朋友们更清楚地了解各地惠民保,我们整理出来了广东省各大城市的惠民保合辑,供大家参考。(以下链接可点击查看投保详情,后附具体介绍)惠民保合辑01广州市——穗岁康、惠民保@官宣!2022年度“穗岁康”参保即将开始!【暖心回归】“广州惠民保2022”正式上线啦!六大升级,保障更全面!02佛山市——平安佛医保参保全攻略,等你查收!一图读懂2022年“平安佛医保”03珠海市——大爱无疆一图读懂!珠海附加补充医保“大爱无疆”,建议收藏!04江门市——邑康保【重磅!】江门人的惠民保障——“邑康保”正式上线!150元保一年,涵盖百万保障!05东莞市——东莞市民保“东莞市民保”2021惠民升级,无需体检、不限年龄...69元保一年!06汕尾市——汕尾善美保一图读懂“汕尾善美保”保障详情!(附个人参保流程)07惠州市——惠州惠医保2022“惠医保”开放参保啦!如何参保?参保信息如何查询?08梅州市——梅州保尚保请收藏!关于2022年保尚保要不要买怎么买,看这篇就够了09湛江市——湛江市民保重大利好!关乎720万湛江医保参保人,湛江首个补充医保升级回归10阳江市——阳江惠民保重磅!阳江首个惠民保正式上线,59元最高享300万保障11茂名市——茂名市民保重磅升级丨2021“茂名市民保”暖心回归,最高保障400万!12揭阳市——揭阳市民保2021年“揭阳市民保”正式上线!保障全新升级!最高保障400万!13汕头市——汕头惠民保“汕头惠民保”项目发布仪式顺利召开!一图看懂“汕头惠民保”!14潮州市——潮州市民保已经有基本医保,还需要买潮州市民保吗?15韶关市——韶关市民保【正式上线】2022年度“韶关市民保”价格不变!保障升级!16河源市——河源市民保关于2022年度“河源市民保”,你想知道的都在这!17肇庆市——肇福保一图读懂肇福保18云浮市——云浮惠民保已经有基本医保,还需要买云浮惠民保吗?19清远市——清远惠民保“清远惠民保”正式上线!20中山市——中山博爱康一图带你看懂“博爱康”21深圳市——鹏城保“鹏城保”上线!99元享350万保障!不限年龄户籍、不限既往症、无需体检!广州市(1)——穗岁康扫码查看《广州市“穗岁康”商业补充健康保险理赔细则(2022年度)》广州市(2)——广州惠民保扫码查看“广州惠民保2022(升级版)产品详情”“广州惠民保2022(基础版)产品详情”佛山市——平安佛医保查看《佛山市商业补充医疗保险赔付责任细则(2022年版)》《2022年恶性肿瘤自费药药品目录公告》珠海市——大爱无疆扫码查看《珠海市附加补充医疗保险恶性肿瘤自费药品目录》《珠海市大爱无疆产品责任细则》江门市-邑康保扫码查看《邑康保保障介绍》东莞市——东莞市民保扫码查看《东莞市民保理赔服务指南》《东莞市民保特定高额药品目录》汕尾市——汕尾善美保扫码查看《“汕尾善美保”保障详情》梅州市——梅州保尚保扫码查看《梅州市商业补充医疗保险“保尚保”产品责任细则》惠州市——惠州惠医保扫码查看《惠州“惠医保”产品方案》湛江市——湛江市民保扫码查看《湛江市民保特定高额药品目录》阳江市——阳江惠民保扫码查看《阳江惠民保保障详情》茂名市——茂名市民保扫码查看《茂名市民保特定高额药品目录》《茂名市民保保障详情》揭阳市——揭阳市民保扫码查看《揭阳市民保特定高额药品目录》《揭阳市民保保障详情》汕头市——汕头惠民保扫码查看《国家谈判医保恶性肿瘤药品目录》《汕头惠民保理赔细则》潮州市——潮州市民保扫码查看《潮州市民保特定高额药品目录》《潮州市民保保障详情》韶关市——韶关市民保扫码查看《韶关市民保特定高额药品目录》《2022年度韶关市民保保障详情介绍》河源市——河源市民保扫码查看《河源市民保特定高额药品目录》《河源市民保保障详情》肇庆市——肇福保扫码查看《15种医保目录外恶性肿瘤药品费用》《肇庆市普惠型商业补充医疗保险“肇福保”保障方案及责任细则(2022年度)》云浮市——云浮惠民保扫码查看《云浮惠民保特药目录》《云浮惠民保保障详情》清远市——清远惠民保扫码查看《清远市普惠型商业补充医疗保险“惠民保”保障方案及责任细则(2022年度)》中山市——中山博爱康扫码查看《门诊特定病种目录》《“博爱康”保障计划详情》深圳市——鹏城保扫码查看《鹏城保详情介绍》《“鹏城保”特定药品清单》以上就是我们整理出来的广东省21个城市的惠民保合辑,供大家查阅,希望能帮助大家更清晰了解惠民保。如有错漏,也欢迎大家补充修正。
 刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心6485人已读
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心6485人已读 - 媒体报道 中国首部,全球瞩目!刘强教授解读“中国年轻乳腺癌专家共识”
https://mp.weixin.qq.com/s/C8rvGi0KYZEf8rK8bH9nIg 编者按:中国乳腺癌患者的一大特征是发病更“年轻”,此类患者的治疗、预后可能有其独特性,而且年轻患者具有更高的生育、美容等特殊需求。然而,当前以西方专家为主导的国际指南共识中,却鲜有关注年轻乳腺癌患者的诊治需求。面对许多尚待填补的“空白”,国际年轻乳腺癌共识(BCY5)专家团中国成员、中山大学孙逸仙纪念医院的刘强教授牵头发起了第一部中国年轻乳腺癌共识的讨论和编写。在共识即将面世之际,《肿瘤瞭望》特邀刘强教授解读该共识的制定历程,分享年轻乳腺癌的诊治进展。 《肿瘤瞭望》:首先我们想请您介绍一下制定“中国年轻乳腺癌专家共识”的背景和意义。 刘强教授:我们知道中国年轻乳腺癌的比例远高于西方国家,这部分人群在治疗需求上有其特殊性,包括生育、卵巢功能保护,且年轻患者预期寿命长,对生活质量要求也更高;再者像一些携带BRCA突变等具有遗传性乳腺癌风险的女性,究竟应该如何选择手术方式来降低同侧和对侧乳腺癌发生率……很多这样的问题,其实在国际指南中也是没有标准答案的,尤其是针对亚洲这样流行病学与欧美有显著差异的人群。 整体上,我们的乳腺癌发病年龄比西方国家提前十几年,绝经前患者比例达60%左右;而西方国家主要发生在绝经后人群中,中位发病年龄为60多岁,三四十岁的患者比例很小,所以在以西方专家为主导的国际指南中,很少关注到这部分人群的治疗需求,很多问题悬而不决,相关研究也不够深入。我在去年参加国际年轻乳腺癌专家共识会议投票(BCY5)的时候发现,很多我们中国或者亚洲年轻患者关心的话题,在欧美为主的专家团里面并没有得到重视,所以我决定要做一个中国版的共识,来解决中国年轻乳腺癌患者的临床困惑。 这个想法一提出来之后,就得到了全国同道的支持和欢迎。有的专家表示,对我们这个共识大会已经期待了一年多。我们开始提出一些问题和想法,希望能够在中国专家的讨论中达成共识,从而指导临床实践,避免年轻乳腺癌患者接受不规范的治疗。这是我们来做这么一个共识的主要目的。 除了得到国内同道的积极响应以外,许多欧美的专家也对我们的共识表达了关注。他们看到我们设计的题目时,表现出浓厚的兴趣,因为他们也很想知道答案,但苦于欧美相应病例数很少,很难在西方国家进行系统研究。他们希望中国的专家共识出台后,能够为国际同道带来参考答案,同时也希望与中国医生开展更多的联合研究,把数据收集起来,获得更高级别的循证医学证据,从而进一步支持和指导我们的临床实践。 《肿瘤瞭望》:正如您所说的,年轻患者的预期寿命长,生育、卵巢功能保护、保乳整形的需求更高。本共识是如何强调年轻患者特殊的治疗目标和治疗需求? 刘强教授:年轻乳腺癌本身就有很多特点,首先年轻乳腺癌往往比年老乳腺癌更高危。我们知道大多数肿瘤的发生、发展可能需要一定的时间积累,从一个肿瘤细胞生长到临床可见、可触及或者有症状的时间大约是10~15年,所以很多肿瘤主要在中老年人中更常见,表面上看起来也是中老年人的患癌风险更高。然而,年轻人一旦罹患癌症,说明肿瘤细胞的发展速度更快,短短3~5年就可以显现出来。 再者,年轻人的免疫力比老年人更强,肿瘤能在短时间能突破年轻人的免疫防线,说明年轻乳腺癌逃脱免疫抑制的能力也很强。综合这些因素来看,年轻乳腺癌的生物学行为可能更差,恶性程度和复发风险也更高。所以在这次会议上我们也会讨论对年轻乳腺癌患者是否需要采取强化治疗,需要采取什么样的强化方案,从而保证此类患者能够获得更高的治愈率。 此外,年轻患者的预期寿命更长,比如我们国家的乳腺癌中位发病年龄是40多岁,这个年纪正是上有老、下有小的时候,她们往往是家庭的顶梁柱,背负的生活压力也很大,对治愈的渴求,以及对提高生活质量,回归家庭、工作岗位、社会的要求也更高。例如,内分泌治疗造成的骨质疏松等不良反应,年轻患者的生育需求、美容需求等都是她们关注的问题。这些特殊需求在年老患者中是不显著的,因而需要我们有别于一般人群的指南共识,尽可能为年轻患者提供科学的、个体化的治疗决策。 《肿瘤瞭望》:“年轻”在HR阳性乳腺癌诊治中尤其受到关注,应该如何考虑此型患者的治疗策略?除了HR以外,年轻患者中是否还有其他特殊靶点/标志物需要被关注? 刘强教授:首先年轻意味着卵巢功能更强,而临床中大多数(70~80%)乳腺癌是雌激素受体阳性的。单从分型来说,年轻乳腺癌跟年老乳腺癌可能没有太明显的区别,但是由于年轻患者的卵巢功能更强,会产生更高的雌激素水平而使ER阳性乳腺癌细胞更容易生长、复发,这也是为什么“年轻”常常在ER阳性乳腺癌中被视为潜在高危因素之一。 在年轻的ER阳性乳腺癌患者中,目前越来越强调通过抑制卵巢功能来降低复发风险。例如,单独使用他莫西芬治疗的ER阳性患者的5年复发风险大约是13-15%;但如果是<35岁的患者,其5年复发风险则高达33%,升高了一倍多。通过加用卵巢抑制(OFS+TAM)治疗,5年复发风险可以降低到21%左右,而应用OFS+AI则可以进一步降低到百分之十几的水平。 除了激素受体以外,BRCA突变在年轻患者中也非常受到关注。一方面是健康女性携带BRCA突变是否需要预防性切除;另一方面是携带gBRCA突变的乳腺癌患者可以从PARP抑制剂治疗中获益,OlympiA研究已经证实,奥拉帕利用于此类高危患者的辅助治疗可以降低复发风险;此外,对于淋巴结转移阳性等高危患者,monarchE研究表明CDK4/6抑制剂辅助靶向治疗也能够降低复发风险。这些强化治疗手段都可以作为年轻患者降低复发风险的潜在方案。所以我们不用对年轻乳腺癌感到恐惧,而是要正确面对,合理利用这些丰富的治疗手段,让年轻患者获得更合理的治疗方案,得到更满意的治疗结局。 《肿瘤瞭望》:不少年轻乳腺癌患者会有“当妈妈”的期望。本次专家共识是如何讨论年轻乳腺癌患者生育需求问题的呢? 刘强教授:确实,临床中有不少年轻患者会来咨询生育相关的问题,尤其现在是晚婚晚育社会,三十多岁还没有要孩子的女性其实很常见。当她们罹患乳腺癌之后,可能需要通过卵巢保护、辅助生殖等措施来满足生育需求。一方面是患者担心这些措施会不会延误或影响乳腺癌的治疗效果,从目前的研究证据来看其实是没有不良影响的。另一方面是如何选择辅助生育方式,比如冻卵、冻卵巢组织、冻受精卵/胚胎等。这次专家共识会议,我们也专门邀请了妇产科、生殖科和乳腺科的医生同台讨论,一起分享和交流对这些问题的看法和经验。 《肿瘤瞭望》:中国年轻乳腺癌专家共识的制定也奠定了我们未来的探索之路,最后请您展望一下未来我们对年轻乳腺癌的研究探索。 刘强教授:其实年轻乳腺癌的很多问题还没有明确答案,主要是缘于其在总体乳腺癌患者中的比例相对较小,这方面的临床数据比较缺乏。即便像我们中国和东亚患者发病相对年轻,35岁以下的年轻患者比例也并不占大多数,在我们的数据库里大约占整体人群的8-10%。在此,我也希望通过“中国年轻乳腺癌专家共识”的制定以及共识会议的召开,能够唤起大家对年轻乳腺癌的重视。 在未来,我希望大家能够齐心协力,收集更多的患者资料,开展更多的多中心协作研究。我们国家的乳腺癌患者基数庞大,每年约有40多万的新发病例,35岁以下的年轻患者数量可以高达数万例,这也是我们相对于西方国家进行此类临床研究的优势。期待在该共识制定以后,我们能够积极开展合作研究,为年轻患者提供更多治疗决策的科学依据。
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1285人已读 - 媒体报道 孕育三胎时确诊乳腺癌,医护团队全程维护母子均安康
https://m.mp.oeeee.com/a/BAAFRD000020220328665771.html?layer=4&share=chat&isndappinstalled=0南方都市报APP
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心160人已读 - 媒体报道 CSCO BC专访 | 刘强教授:从亡羊补牢到未雨绸缪——三阴性乳腺癌的早期治疗新策略
https://mp.weixin.qq.com/s/NPa-lvoHc-_FKC5gdF-GmQ"全国乳腺癌大会暨中国临床肿瘤学会乳腺癌(CSCOBC)年会"于2022年4月8日召开。本次会议邀请了
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1514人已读 - 媒体报道 2022 CSCO BC|刘强教授:用精准治疗卸下TNBC患者的悬顶之剑
https://mp.weixin.qq.com/s/xZmIw0qbGhjUxFMM71OAFA编者按在2022年CSCOBC年会上,中山大学孙逸仙纪念医院的刘强教授带来“基于转化研究的三阴性乳腺癌早期治疗策略”主旨报告。刘强教授在线上接受我们的采访中表示,术后近期复发率高、预后差、治疗手段单一是三阴性乳腺癌(TNBC)临床治疗的痛点,使其成为高悬在患者头上的达摩克利斯之剑,让许多患者比较焦虑。为了进一步提高早期TNBC患者的治愈率,刘强教授团队进行了许多转化研究,包括利用ctDNA进行早期乳腺癌预后及疗效的监测等,这种早期监测手段对TNBC的升、降阶治疗均有重要指导意义。01《肿瘤瞭望》:三阴性乳腺癌(TNBC)被认为是“最凶险”的乳腺癌亚型,请您简要为我们介绍一下,早期三阴性乳腺癌在临床治疗方面还存在哪些痛点?刘强教授:很多病人和医生都对TNBC谈之色变,主要是由于TNBC的临床治疗存在以下几方面痛点。首先是TNBC的复发风险,尤其是近期复发风险很高,其两年内的复发转移风险高达8~10%,远高于其他亚型乳腺癌的同期复发风险。我们在临床上也遇到不少这样的TNBC病人,辅助化疗刚刚结束才几个月甚至还没等到辅助化疗完成,就发生复发转移。这些多是因为原发耐药和化疗无效导致的。其次是治疗手段单一。我们知道HER2+、HR+乳腺癌,除了化疗以外还有都相应的靶向或内分泌治疗手段,而TNBC尤其是早期辅助治疗领域仅仅有化疗这一类治疗手段,而且一小部分TNBC患者对化疗并不敏感,也就是存在原发耐药。我们中心对近1800例接受新辅助化疗的早期乳腺癌患者进行的回顾性分析发现,有将近20%多的TNBC患者在新辅助化疗期间发生进展或疗效不佳,这部分患者的肿瘤其实是化疗打不动的、是化疗无效的。再者是TNBC一旦发生复发转移,患者生存期短、预后极差。据统计,TNBC早期患者两年内的死亡风险是同期HR+/HER2-乳腺癌的8-11倍,所以有很多TNBC患者确诊后会担心肿瘤一下子就复发转移了。从最近欧洲大规模的晚期治疗数据来看,HR+和HER2+转移性乳腺癌患者的总生存仍可达40个月以上,HER2+患者甚至可达50多个月,而TNBC患者的总生存平均仅有十几个月。临床上,虽然大多数三阴乳腺癌还是可以彻底治愈的,但是其复发风险仿佛高悬在病人头上的达摩克利斯之剑,不知道什么时候会不会发生,让许多病人心里感到焦虑不安。总之,TNBC术后近期复发率高、治疗手段单一、转移后预后很差,是目前临床诊疗的最大痛点。02《肿瘤瞭望》:针对临床治疗中存在的这些痛点,我们应采取哪些措施,以提高早期三阴性乳腺癌的治愈率?刘强教授:TNBC确实是比较难治的,但它主要是短期复发风险,即前两三年的复发风险比较高,而5年以后的复发风险反而低于其他亚型。此外,早期TNBC的整体治愈率也不能算低,可以达到60~70%以上的完全治愈。因此,TNBC患者不必太过恐慌和焦虑,心理压力增加可能会影响自身免疫力,反而增加肿瘤复发风险。也就是说我们要做好病人的心理建设,做到对疾病知己知彼,对治疗有的放矢。这其中最重要的是要精准判断TNBC患者的复发风险。我们在临床上发现,TNBC的复发转移风险与肿瘤大小、淋巴结转移等临床特征的相关性明显不如其它亚型乳腺癌;即便肿瘤体积较小、没有淋巴结转移,也可能发生全身转移,而且肝、肺、脑等内脏转移很常见。由此可见,对于TNBC患者需要应用更多新的手段来评估复发转移风险。首先,可以考虑利用新辅助治疗的药敏平台作用,来判断患者的预后以及药敏信息,从而指导术后辅助治疗。正如前面提到的,我们中心的数据显示有超过20%的TNBC对化疗不敏感,我们的病人也常常提问“怎样才能知道化疗是不是有效”,新辅助治疗正是比较好的手段。目前,整体上TNBC的pCR率为30~50%,这部分患者的预后要显著好于non-pCR患者。CREAT-X研究已经证实,对于non-pCR的高危患者,给予卡培他滨强化辅助治疗,可以将5年DFS率从56%提高至70%。当然,达到pCR也并不代表就可以高枕无忧,仍有百分之十几的患者会发生复发事件。那么,怎样才能进一步精准地筛选出高危患者,或者给予更精准的风险监测?我们的研究团队应用了一种全新的液体活检手段——循环肿瘤DNA(ctDNA)。众所周知,几乎所有肿瘤都是由基因突变驱动的,ctDNA正是检测肿瘤释放到患者血液循环中的突变DNA,从而提前发现可疑全身复发转移的患者。我的课题组从2014年就开始研究ctDNA,发现ctDNA可以很好地预测早期乳腺癌新辅助治疗的疗效和预后,该研究成果于2020年发表在ASCO官方期刊JCOPrecisionOncology杂志上,文章发表后引起广泛关注,也被ASCO评为“TOParticlesin2020”之一,即2020年度最受欢迎的文章之一。国外的其他一些论著和综述也纷纷引用了我们的文章,正如一篇引用我们文章的综述所写的,未来乳腺癌到底是局部性疾病,还是全身性疾病,也许就是由这样一个可以判断全身肿瘤负荷的检测来决定。乳腺癌的生物学异质性很大,有的肿瘤倾向于全身转移,有的则局限于原发灶部位;而ctDNA这种液体活检可以很好地、提前捕捉到肿瘤向全身转移的迹象。我们正在进一步进行扩大样本的前瞻性研究来验证这一精准诊断工具,目前已经积累了300多例患者的数据,相关论文正在撰写之中。△刘强教授团队发表于JCOPrecisionOncology的研究近年来,TNBC的强化治疗策略越来越受到重视,虽然当前的主要治疗选择仍是化疗,但已经涌现出了PARP抑制剂、PD-1免疫检查点抑制剂等新治疗手段。然而,这些治疗手段也有其局限性。尽管KEYNOTE-522研究证实PD-1抗体联合化疗用于早期高危TNBC患者(新)辅助治疗,可以显著提高患者5年EFS率,但免化联合的严重AE率高达34.1%,而且有4例治疗相关导致的死亡,因此治疗的安全性和耐受性仍是医生和患者所不能忽略的。此外,我们从2017年开始通过转化研究的发现,开展了针对晚期三阴乳腺癌的患者采取低剂量抗血管生成联合免疫的临床研究,结果发现可以带来相当不错的治疗效果,其中不少是肝、脑、肺转移的患者,部分病人得以长期生存,最长的PFS已经达到了51个月之多。强化治疗的确可以使一部分高危患者增加获益,关键在于如何早期筛选出这部分患者,ctDNA或将是有潜力的方法。实际上,ctDNA不仅可以做“加法治疗”,也可以做“减法治疗”。我以自己接诊过的两例患者来举例说明。一例是上个月再次来门诊找我随访的ER阴性患者,她还给我送了一幅锦旗表达谢意,因为已经满5年了还没有复发。这例患者的治疗过程正是利用ctDNA指导“加法治疗”。我们在2017年对患者进行新辅助后的肿瘤根治手术,术后病理可以看到淋巴结转移负荷很高,之前的疗效欠佳,于是我们建议患者进行ctDNA监测。在术后不到1年的时候出现ctDNA阳性,提示有全身复发转移的倾向,所以我们及时给予强化治疗,随后ctDNA也转阴了。强化治疗一年停药半年后ctDNA又复阳了,而且丰度逐渐增加,我们也是及时给予强化治疗,ctDNA又转阴了,患者目前已经存活超过了5年多,至今没有复发转移。第二例是一位83岁高龄的TNBC患者,Ki-67指数达到80%,有8枚淋巴结转移,临床上应当属于高危患者。但考虑到高龄,患者可能耐受不了强化治疗。我们在根治术后对患者进行液体活检发现,患者的ctDNA为阴性,也就是说该患者的肿瘤可能更倾向于侵犯局部或区域组织,所以术后我们并没有采取强化治疗,而是选择白蛋白紫杉醇周疗这样毒副作用更小的方案,患者顺利完成了12周的化疗。目前患者已经术后存活了2年多,没有任何复发转移。总之,提高早期TNBC的治愈率,我们需要更精准的风险评估、监测手段,需要更丰富、更有效的治疗手段。正如那篇引用我们文章的综述所描述的,未来判断乳腺癌到底是局部疾病还是全身疾病,需要这种更精准的手段。希望我们正在开展的ctDNA指导下的早期三阴乳腺癌患者的多中心临床研究,能够为TNBC患者提供更精准的预后评估和升级治疗,尽量让三阴乳腺癌患者在早期得到最大可能的治愈机会。
 刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1097人已读
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1097人已读 - 媒体报道 南方人物周刊 - 时代医者:看清来路,照亮前路
https://mp.weixin.qq.com/s/e6NLmr8DSrukGI1jlAI_5A 过去很长的一段时间里,治疗手段的缺乏、辗转求医的奔波、可望而不可及的进口药品让肿瘤病房的故事被隐藏在
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心399人已读 - 精选 大咖Q谈 | 刘强教授畅聊乳腺癌精准诊疗中的MRD检测
https://mp.weixin.qq.com/s/AvknKKGFEjvbOlqYnmUNsA MRD检测除了能告诉我们病人预后好或者差之外,接下来还会有更多的研究数据指导我们,如何根据MRD数据给予患者最佳的精准治疗策略,包括加强治疗或者降级治疗,这是MRD在未来个体化精准治疗中的一个发展方向。 ——刘强教授 为探讨和推动MRD在临床的应用,吉因加特别策划《大咖Q谈》栏目,邀请肿瘤诊疗领域顶级专家,接龙畅谈MRD检测的临床应用。本期节目中,乳腺癌领域的专家,中山大学孙逸仙纪念医院的刘强教授接受陆舜教授的邀请,分享了MRD在乳腺癌中的精准诊疗意义。 Q1 如今MRD在实体瘤领域越来越受到关注,并且屡次被验证可预测围手术期治疗疗效及复发风险。从乳腺癌的角度,您是如何看待MRD这个指标的? 刘强教授:首先,我们知道实体肿瘤跟血液系统的肿瘤一直是有很多不一样的地方,血液系统的肿瘤不局限于局部,因此可以比较容易地通过血液来查到肿瘤的状态。但是实体肿瘤,在以前它只是被认为是一个局部疾病,比如肺癌、胃癌、肝癌、乳腺癌,都是以所发生的解剖部位来命名,而这些实体肿瘤以前的治疗都是手术为主,因为只是在局部能看的见肿瘤,当然手术切除是最关键的。不过近年来越来越多的研究发现,对于实体肿瘤单纯手术切除可见的肿瘤是不够的。这是因为,在人体里还有一些少量的影像学还不可见的这些肿瘤细胞残存在那里,这会引起肿瘤的复发和转移。这就是近年来比较火热的一个概念叫做MRD,叫Minimal Residual Disease。 其实今天实体瘤的治疗的理念已经到了一个更精准更精细化的一个程度,单纯的手术切除可以说是不能满足大多数实体肿瘤的需求,尤其是乳腺癌。乳腺癌现在已经超过肺癌成为世界第一大肿瘤,在中国每年乳腺癌发病42万,死亡达到12万之多。死亡的12万里有些一开始就是晚期,但更多的是原来是早期乳腺癌,即使经过了比较强大的系统治疗之后还是产生了复发和转移,由于肿瘤细胞的耐药导致治疗没有办法彻底治愈疾病,进而导致病人的生命受到了威胁。那么我们怎么样去知道手术之后哪些人是有这种残留的肿瘤的存在,也就是MRD的存在,这是非常非常重要的。也就是说以前我们只能根据影像学来判断病人早期还是晚期,没有远处转移我们都叫做早期,只要有远处转移就定义为晚期。 实际上只要影像学一旦发现转移,基本上就是一个不可治愈的疾病,这点对于病人来说是非常大的一个打击。那我们怎么样去避免让那些影像学还没有发现转移的病人,也就是早期的病人不去进展到晚期,这一点就是如何提高乳腺癌治愈率的关键。但是我们又不能够对所有的病人去不分青红皂白的去加强治疗,所以我们怎么样去筛选真正高危的病人去加强治疗,这一点是非常重要的。乳腺癌的治疗手段是非常多的。除了手术之外还有化疗、放疗、内分泌治疗、靶向治疗、免疫治疗等等一系列的治疗。那这些治疗怎么样去组合,来高效地精准地用于那些高危的乳腺癌患者,来尽量提高他们的治愈率,这是一个关键。 首先就是怎么识别这种病人?我们去年发表在JCO精准肿瘤学上的这篇文章就引起了很大的轰动,美国很多医生和研究者都纷纷在推特等社交媒体上转载这篇文章。其中有一个推特评论挺有意思,她说“I wish this had been available in 2011 ?”。我估计这位推特的转发者就是在遗憾这样的技术如果早点有就好了,如果早有,就可能挽救患者的生命。我们这个技术首次证实了,在早期乳腺癌患者里,我们通过血液的循环肿瘤DNA的高灵敏度的高精度的大范围的一个检测技术,能够很好地预测病人治疗的疗效以及筛选出高危的病人。也正是这个研究,为我们正在进行的一个大型的随机对照临床研究奠定了一个坚实的基础。这些技术确实是近几年才开始慢慢走向临床应用。我们之前的技术不够成熟,成本过于昂贵,阻止了这个技术很好的应用于临床。 但是近年来突飞猛进的技术革新让成本也大幅度下降,然后技术也达到更加灵敏更加精确的一个程度,所以MRD的这个概念才在近期被提出来,而且在各大实体肿瘤都是一个非常新而且非常热门的一个概念。通过外周血ctDNA检测是目前检测乳腺癌MRD的主流技术方案,但不是所有ctDNA检测都可以用于MRD检测,早期实体瘤外周血ctDNA的丰度远低于晚期肿瘤,因此需要更高敏感性和更具特异性的检测方法。 Q2 在临床上您会更倾向于于建议哪种亚型的乳腺癌患者做MRD检测?什么时机去做?或者说您推荐在哪些检测节点去做? 刘强教授:这个就说到了试验技术的一些具体细节方面了。我们知道血液的一些指标的检测是能够帮助我们MRD的一个早期的辨认,但是什么样的病人最适合以及什么时间来做,是很多临床医生所困惑的问题。首先在我们那个研究里面,我们的发现是,ER阴性的病人是更容易出现ctDNA阳性的,这一点跟ER阴性的病人容易出现早期的复发转移是相符合的。ER阳性的病人我们知道他的短期的复发风险并没有ER阴性那么高,但是他长期的风险也并不低,尤其是骨转移的风险是相当的高的。其次我们在什么时候做检测呢?我们主张是在治疗之前做检测,那个点是最灵敏的。因为治疗之后,比如化疗手术、放疗、内分泌治疗这些等等就可能导致他的假阴性。但是在治疗之后如果原来是阳性后来转阴了,这也是一个好的消息,如果能一直维持转阴,那相信这个病人是对治疗相当敏感的。这也是病人治疗有效的一个标志,也是预后比较好的一个标志。所以我认为首先对于ER阴性的病人来说更有意义,因为ER阴性的病人不少都是在手术短期内三年之内就复发转移。这是第一点。 第二点这些病人也经常有一个疑问或者抱怨,明明三个月之前检查什么问题都没有三个月之后就发现全身转移了,而且这种转移往往来的特别快。因为ER阴性的肿瘤它的增殖的指数是更高的,也就是说肿瘤细胞翻倍的时间是更短的。所以这个肿瘤细胞确实容易在短期内出现复发和转移。 另外一点我会倾向于在觉得这个病人是高危的情况下或中高危的情况下,我会尽可能在治疗之前就去做检测,但是即使病人错过了治疗前的时间点,也并不是说治疗之后就没有意义。如果病人治疗之后的点ctDNA还是阳性,那说明这个风险就更高一些。但是治疗之后的点如果是阴性也不能掉以轻心,有可能是这个治疗之后带来的甚至短暂的假阴性。如果治疗之后的时间点还是阳性的话,那就告诉我们这个治疗有可能是效果不好,我们需要及时更改方案。 Q3 对于您正在进行的这项多中心、开放设计,ctDNA 在三阴型乳腺癌患者新辅助治疗中应用的临床研究,您希望实现哪些目标? 刘强教授:我们去年发表在JCO精准肿瘤学上的那篇文章报道了循环肿瘤DNA的预测价值,预测病人预后的价值。但是能不能够对病人的治疗产生影响?能否通过这个检测让我们把预后原本较差的ctDNA阳性病人提高治愈率?这是我们正在做的一个随机对照临床研究的探索。这个研究是目前中国第一个,也是唯一一个,根据循环肿瘤DNA来决定乳腺癌病人术后是否需要加强辅助治疗的一个随机对照临床研究,应该说是非常有意义。之前的研究我们知道阳性的病人术后预后比较差,那我们能不能做什么来帮助她们把预后提高呢?这就是我们正在做的这个研究。 希望通过我们的这个研究,能够奠定一个早期的MRD的检测或者循环肿瘤DNA的检测标准,能够帮助我们精准的筛选病人,一些低危的可以不用加强治疗,放心的让她们用标准治疗就够了,而中高危病人不能掉以轻心,我们必须要加强治疗来尽量提高她们本来相当差的一个预后,或者说比较高的一个复发风险我们来尽量降低。这个研究目前已经在全国多个中心开始开展,目前已经入组了一百多位患者,进展相当不错。全国各地的病人也都踊跃地积极参与,因为能有这么一个机会来知道自己的风险到底有多高,而且还有可能改善预后,这对于我们入组人群也就是三阴乳腺癌的患者,是一个很大的福利和福音。 Q4 如果要把MRD检测形成乳腺癌患者检测的临床常规,您认为还需要哪些工作推进? 刘强教授:自然是更多的研究数据。近年来包括我们还有国际上一些课题组都纷纷证实了这个早期MRD的检测是具有良好的预后预测价值的,也就是复发风险的预测价值的。但是目前很遗憾,在乳腺癌领域还没有一个研究去证实它有一个对治疗或预后有影响的价值。我们正在做的这个III期临床研究,当然我们首先是希望这个样本量的扩大能够让我们更精准地知道哪些病人用这个检测是最需要的最有效的。毕竟这个检测不是免费的,而且还是价格不菲的一个检测。当然在今天来说,已经是很多病人能负担得起的,但毕竟还是有一定成本的。我们希望能够最精准的用到最需要的病人身上,这是第一点。 第二点我们希望扩大检测的价值就是除了它能告诉我们病人预后好或者差之外,还能够告诉我们这个病人如果预后差,能不能够去给他最精准的治疗最有效的治疗来提高她的预后?还有一点,可能有些比较容易忽视的一点,就是如果病人的预后足够好,那是不是能够降级治疗比如是不是可以不做化疗?因为我们都知道乳腺癌里面有一部分病人,少部分病人目前是可以被免除化疗的,但是大多数病人还是不能被免除。很多病人都会对化疗有一个很恐惧的理念,但其实我们作为医生认为并没有必要去那么恐惧。因为我们今天乳腺癌的化疗基本上耐受都还是很好的,不会引起什么严重的副作用。当然对病人来说,如果能够避免不必要的伤害那当然是更好啊。 举个例子来说,我们前不久有一个83岁的老太太,三阴乳腺癌8个淋巴结转移,这种情况下我们一方面太强的治疗肯定不行的,因为老太太已经83岁了,她身体很棒但是再棒也是一个老年人的状态。那对于这种患者我们要去用跟年轻人一样方案显然是不现实的。而我们也知道这种三阴乳腺癌细胞有的是很喜欢往外面跑,通过血液往全身跑。有的即使没有腋窝淋巴结转移但全身转移发生都不少见。而有的肿瘤又反过来只喜欢在局部转移,不喜欢到全身去这种情况。我们给这个老太太做了一个基因检测,就刚好发现它就是那种肿瘤喜欢在局部去长,血液里面完全是阴性的,而且在治疗之前就完全是阴性的。那这一点就告诉我们她的复发风险并不高,于是我们就给她做了降级的化疗。目前至少病人的情况都还非常好,耐受性也很好,所以我想精准治疗接下来会给我们带来越来越多的个体化的最有效的副作用最小的治疗手段。
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心1294人已读 - 学术前沿 从晚期到早期,OlympiA研究报道奥拉帕利给gBRCA突变早期乳腺癌提供更高治愈机会!
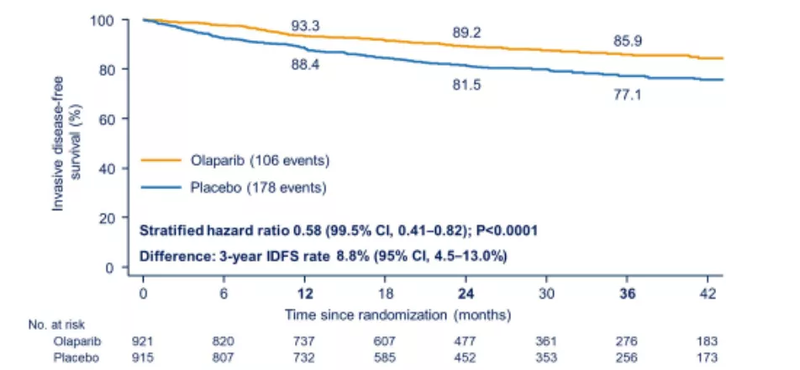
转自:良医汇-肿瘤医生APP https://mp.weixin.qq.com/s/DDgc4ltIWpkNT3OUprygkg 2021年美国临床肿瘤学会(ASCO)年会上,OlympiA研究作为LBA1重磅发布,奥拉帕利成为gBRCA突变早期乳腺癌的首个靶向精准疗法,有望改变早期乳腺癌治疗格局。2021年6月12日,阿斯利康第十六届“经典全程 得领未来”乳腺癌高峰论坛上,中山大学孙逸仙纪念医院刘强教授就“2021 ASCO gBRCAm早期乳腺癌精准治疗进展”做了精彩报告。会后,【肿瘤资讯】对刘强教授进行专访,对OlympiA研究的数据解读,研究的价值和意义,及未来探索方向等问题做出深度分享。 2021 ASCO gBRCAm早期乳腺癌精准治疗进展 BRCA1/2基因突变使乳腺癌风险提高5倍。BRCA突变可导致同源重组修复通路缺陷(HRD),DNA损伤修复受损而使得肿瘤几率增加。而PARP抑制剂则可通过“合成致死”效应而导致BRCA突变肿瘤细胞死亡。奥拉帕利引领了针对BRCA的精准治疗,其在BRCA突变多种实体瘤中均取得优异疗效,先后10次成功登顶国际顶级医学期刊《新英格兰医学杂志》。2017年,OlympiAD研究中,奥拉帕利对比化疗治疗接受过化疗或内分泌治疗的gBRCA突变晚期乳腺癌,两组的中位无进展生存期(PFS)分别是7.0个月 vs 4.2个月(HR=0.58,P<0.001),客观反应率(ORR)更是提高了一倍到60%,因而获批适应证。2021年ASCO 公布的OlympiA研究则将奥拉帕利的应用向早期乳腺癌推进了一大步。 这是一项Ⅲ期多中心随机安慰剂对照研究,1836例高危gBRCA1/2突变/HER2-早期乳腺癌患者,局部治疗及辅助/新辅助治疗后,1:1随机接受奥拉帕利或安慰剂治疗1年,主要终点为无浸润性疾病生存(iDFS),次要终点包括无远处疾病生存(DDFS),总生存(OS),BRCA1/2相关癌症发生率,生活质量和安全性。 奥拉帕利组和安慰剂组的3年iDFS率分别是85.9% vs 77.1%(HR=0.58,P<0.0001),绝对iDFS获益达到8.8%(图1)。两组3年DDFS分别是87.5% vs 80.4%(HR=0.57),绝对获益达到7.1%(图2)。两组3年OS率分别是92.0% vs 88.3%(HR= 0.68,P=0.024),OS表现出获益趋势(图3)。 图1研究的 iDFS分析 图2 研究的DDFS分析 图3 研究的OS分析 奥拉帕利不良事件(AE)与已知一致。两组≥3级不AE发生率分别是24.3% vs 11.3%,严重AE发生率8.7% vs 8.4%,导致永久停药的AE发生率分别是9.9% vs 4.2%,导致死亡的AE发生率分别是0.1% vs 0.2%,显示出可控的安全性。奥拉帕利对患者生活质量无显著影响。 总体而言,OlympiA入组的高危HER2-/gBRCA突变患者,经过标准治疗后依旧有较高的iDFS和DDFS风险。局部治疗和新辅助/辅助化疗后,1年的奥拉帕利辅助治疗显著提高iDFS和DDFS。奥拉帕利组发生死亡事件的患者数更少,但在中位随访仅2.5年时,OS获益尚没有达到第一次中期分析时预设的显著性水平(P<0.01),盲态随访还将继续。奥拉帕利安全性良好,AE可控,不影响整体患者报告的生活质量。基于OlympiA研究结果,可以预期gBRCA1/2基因检测将成为早期HER2阴性乳腺癌的重要生物标志物。 专家点评 奥拉帕利显著提高治愈机会,成为高危gBRCA突变早期乳腺癌患者治疗的强力武器 刘强教授:BRCA基因突变患者发病年龄比较轻,疾病分级更高,但是大多数研究显示在经过充分的治疗之后,BRCA患者预后并不亚于无BRCA突变患者。BRCA突变患者还存在许多未被满足的临床需求,尽管已知BRCA突变存在,有PARP抑制剂这样有效的靶向药物,但是如何选择合适的用药患者一直不清楚。PARP抑制剂治疗晚期gBRCA突变患者获得了PFS的延长和客观反应率(ORR)的提高,但是能不能应用于早期患者,早期患者中应该用于新辅助还是辅助治疗,是否应该用于高危患者,比如新辅助治疗未达到完全病理缓解(pCR)的患者,一直是还没有答案的问题。今年ASCO上公布的OlympiA研究就回答了相关问题。该研究将PARP抑制剂从晚期向早期应用推进了一大步。早期高危患者要强调尽可能提高治愈率,因为一旦复发转移就几乎不可治愈。在提高治愈率方面,PARP抑制剂提供了非常有效的强力武器,因此PARP抑制剂在BRCA突变早期患者中极具治疗潜力。 BRCA突变患者应用奥拉帕利获益显著,OlympiA研究具有巨大价值 刘强教授:这项研究影响重大。OlympiA研究作为2021 ASCO的LBA公布,并同期发表在《新英格兰医学杂志》,反映了该研究的重要性。之前BRCA突变检测有助于预测对侧乳腺癌、卵巢癌、和保乳术后同侧复发风险,而在治疗上并没有相应的指引,这一直是困扰着患者和临床医生的问题。OlympiA结果的公布把针对BRCA突变的有效靶向药物推向了早期,尽管仅进行了3年左右随访,但是结果非常惊艳,iDFS和DDFS得到显著提高。研究提醒我们,对于早期高危BRCA突变患者,PARP抑制剂是非常有效的选择。 研究是在2014年开始入组的,在今天很多治疗已经有了一些改变,比如说早期三阴性乳腺癌(TNBC)新辅助治疗后未达到pCR的患者,术后卡培他滨强化辅助治疗可以提高患者的治愈几率。如果患者携带BRCA突变,到底应该使用卡培他滨还是PARP抑制剂?我认为奥拉帕利应该比卡培他滨更有效,是高危BRCA突变TNBC患者加强辅助治疗的更佳选择,其原因有三: 首先,在奥拉帕利对比化疗治疗晚期患者的OlympiAD临床研究中,化疗组42%的患者使用了卡培他滨,PFS仅为4.2个月,而奥拉帕利的PFS达到7个月以上,ORR也显著提高,提示在BRCA突变患者中,PARP抑制剂的有效性高于卡培他滨。 第二,2019年报道一项小样本研究,PARP抑制剂单药用于早期BRCA突变TNBC患者的新辅助治疗, 24周的pCR率高达50%左右,今年ASCO会议报道更大样本的NEOTALA研究,pCR率同样接近50%,而卡培他滨单药新辅助化疗pCR率不可能达到50%,因此可以间接来推论PARP抑制剂在BRCA突变患者的疗效优于卡培他滨。 第三,PARP抑制剂是靶向治疗,和化疗完全不一样。化疗耐药后往往是多药耐药,如果新辅助化疗对蒽环类和紫杉类效果不那么好,没有达到PCR,卡培他滨的疗效同样有限。而靶向药物奥拉帕利的作用机制完全不一样,化疗药物耐药后可能敏感性依旧保持,所以综合来说,PARP抑制剂对BRCA突变早期乳腺癌患者的效果应该优于卡培他滨。 研究同时入组了不到20%的激素受体(HR)+/HER2-、淋巴结转移数目≥4的高危患者,此类患者同样有明显获益的趋势。但是该研究一开始主要入组TNBC患者,一年半之后才改为可以入组HR+患者,每组的HR+患者只有160例左右,3年随访时间还没有把这部分患者的复发高峰包括进去,所以尽管这部分患者具有良好的获益趋势,但样本量太小,随访时间太短,目前还无法得到让人非常信服的证据,尤其对于这部分患者来说,CDK4/6抑制剂加强辅助治疗也是有效的选择之一。但是大家一致认同奥拉帕利对于BRCA突变患者是非常有效的药物,对于新辅助未达到pCR,以及高危患者的辅助治疗都具有良好的前景和价值。 精准检测是精准治疗的基础,合理扩大获益人群是未来探索方向 刘强教授:如何提高高危早期患者的治愈率是大家始终关心和不断探索的问题。PARP抑制剂从晚期进入早期令人鼓舞,早期患者将有更高治愈率,拥有了更为有效的治疗选择。同时BRCA突变患者数量较少,而具有PALB2、ATM等HRD相关基因突变或BRCA低表达可能同样对于PARP抑制剂敏感。如果能够进行更精准的多基因检测,将有助于拓展获益人群。例如TBCRC 048研究就显示gPALB2突变患者使用奥拉帕利的ORR可以达到80%,而体细胞BRCA1/2突变患者的ORR也可以达到50%,表明PARP抑制剂的适应证将来不只是gBRCA突变,希望适应证能够进一步拓宽,使更多患者获益。 我们中心目前的研究发现部分药物可以显著降低BRCA表达,人为造成BRCA相关功能缺失,使之获益于PARP抑制剂,因此人为诱导BRCA功能缺失将是未来探索方向。另外还可以探索PARP抑制剂是否可以用于gBRCA突变携带者的预防。因为OlympiA研究中,奥拉帕利显著降低了卵巢癌等第二原发癌的发生率,所以奥拉帕利可能可用于gBRCA突变携带者的癌症预防,这需要更大样本的研究和更长的随访来告诉我们确定性结果。 综上所述,对于奥拉帕利的期待: 第一,希望适应证更广,能够让更多携带BRCA突变的人获益,包括胚系突变患者的肿瘤预防。 第二,能够拓展到无BRCA突变但是有HRD的患者,甚至人为诱导BRCA缺陷的患者中,这样可以大大提高药物应用价值和获益人群。 第三,药物的应用有赖于精准检测,规范化基因检测和高危人群的筛选是达到药物有效性最大化的关键。希望有更多患者获益,但是又尽可能不给更多患者带来治疗副作用,所以规范化基因检测非常重要。欧美国家对NCCN指南指定人群的基因检测率也不足50%,如果中国能够推广检测,以及HRD的检测如果能够进入相应人群的医保,能够极大提高检测率,增加获益人群,推广好检测是药物良好应用的前提。
 刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心2141人已读
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心2141人已读 - 精选 刘强教授:开启免疫之窗,为三阴性乳腺癌患者增加一线希望
https://mp.weixin.qq.com/s/9-MkIBCBRm18F1Zwt2UYvQ在乳腺癌各亚型中,三阴性乳腺癌可谓是“最毒、最凶“的一个类型,复发转移最快,转移后生存期最短,让许多患者对三阴乳腺癌都颇为恐惧。当三阴性乳腺癌遇上免疫治疗,这种新疗法能否为三阴性乳腺癌患者增加一线希望?中山大学孙逸仙纪念医院乳腺肿瘤中心刘强在国内率先开始乳腺癌免疫治疗的转化和临床研究,并报道了乳腺癌中抗血管生成和免疫联合治疗的突出疗效,三阴性乳腺癌免疫治疗领域的国内先行者——中山大学孙逸仙纪念医院刘强教授在2021年4月9日召开的全国乳腺癌大会上做了乳腺癌免疫治疗的专题演讲,并于会后分享了他的临床经验和免疫方案的研究历程。三阴:最可能获益于免疫治疗的分型三阴,是指雌激素受体(ER)、孕激素受体(PR)、人表皮生长因子受体-2(HER2)表达均为阴性。刘强教授分析了这种疾病之所以棘手的原因:一是治疗手段单一,一般不适用内分泌治疗或靶向治疗,而主要的化疗对部分病人效果欠佳,尤其转移后化疗很容易耐药;二是肿瘤侵袭性强,术后两三年内的复发风险较高;三是一旦出现复发转移,患者的生存预后非常差。欧美的研究数据显示,复发转移的三阴性乳腺癌患者的中位总生存期(OS)仅为15~18个月,远低于HER2阳性和激素受体阳性患者。与传统化疗难以延长患者总生存期不同,免疫疗法较大幅度地延长了晚期三阴性乳腺癌的总生存期,甚至少数患者有望得以长期生存。刘强教授分析了免疫治疗和既往治疗模式有何不同:“免疫治疗属于扶正,正气存内,邪不可干,以不变的免疫系统来对付善变的肿瘤细胞,变被动为主动。肿瘤免疫治疗的目的是激发和调动机体的免疫系统,改变肿瘤微环境,提高抗肿瘤的免疫力,从而控制和杀伤肿瘤细胞。”而对于为何免疫治疗在三阴性乳腺癌上可以取得奇效,刘强教授表示,乳腺癌传统上被认为是一种冷肿瘤,与黑色素瘤、肺癌等肿瘤相比,肿瘤突变负荷较低、抗原较少。然而,三阴性乳腺癌相比其他亚型乳腺癌有更多肿瘤浸润淋巴细胞(TILs)。同时,该类肿瘤尤其BRCA突变者又有较多基因突变,可产生肿瘤特异性新抗原,可激活肿瘤特异性T细胞产生抗肿瘤免疫反应。此外,三阴性乳腺癌的肿瘤和免疫细胞上均有较高水平的PD-1/PD-L1表达,为免疫治疗提供了直接靶点。“因此,三阴性乳腺癌患者是最可能获益于免疫治疗的乳腺癌人群。”刘强教授说。聚焦免疫联合抗血管生成治疗尽管免疫治疗从机制上说是治疗三阴性乳腺癌的理想药物,但需要正视的是,单用免疫检查点抑制剂的治疗有效率相当低,因此全球研究人员探索了多种联合方案来提高反应率。从既往的相关研究来看,IMpassion130研究显示出免疫联合白蛋白紫杉醇化疗确有OS上的获益,但采用紫杉醇的IMpassion131研究却是阴性结果。刘强教授提醒:“并非所有化疗药都可以被用来进行联合,需使用那些事前不用激素预处理的化疗药物,以免激素药物抑制机体的免疫功能。”另一方面,免疫联合其他免疫疗法、联合靶向治疗虽然也获得了一些成果,但许多还只是小样本研究,结果并未让人十分满意。在刘强教授看来,免疫与抗血管生成药物的联合可能是众多免疫联合方案中的最佳选择。其本人也是全球最早报道免疫联合抗血管治疗三阴性乳腺癌的研究者之一。2017年,刘强教授的博士生李倩在前期研究的动物模型中观察到抗血管生成和免疫治疗具有非常好的协同作用。当时,Science Translational Medicine背靠背发布的两篇文章和这项研究结果高度一致,这促使刘强教授最早开展了免疫联合抗血管生成的研究。2019年,刘强教授团队发布在Clinical Cancer Research的研究进一步发现,低剂量抗血管生成药物可改善肿瘤微环境,比如肿瘤的血管壁不完整,组织间压比较高,淋巴细胞等免疫细胞难以进入。而低剂量抗血管生成药物导致的血管正常化可改善这种情况,从而促使更多的免疫细胞进入肿瘤组织,逆转原本抑制免疫的肿瘤微环境。为何将研究方向锁定在免疫联合抗血管生成治疗上?刘强教授表示,主要是因为二者存在协同机制,抗血管治疗可以重新编程肿瘤的免疫微环境,这就更有利于免疫检查点抑制剂发挥强有力的疗效。“过去不可想象的疗效”那么,实践中免疫联合抗血管生成疗法对三阴性乳腺癌的疗效又如何呢?据刘强教授介绍,其与中山大学孙逸仙纪念医院宋尔卫院士共同主导了一项II期临床研究,旨在探索PD-1抑制剂卡瑞利珠单抗联合抗血管生成药阿帕替尼的无化疗方案治疗晚期三阴性乳腺癌。在刘强教授看来,该方案在三阴性乳腺癌的治疗中属独辟蹊径。“因为不用化疗,这是研究的创新和亮点。”刘强教授说。据悉,这项研究的连续给药组纳入30例患者(卡瑞利珠单抗 200 mg每两周一次+阿帕替尼250 mg每天一次,d1~14),入组人群有较多二线、三线患者。联合方案的疗效较免疫单药有大幅度的提高,客观缓解率达到43%,且安全性良好。目前除10%的患者失访外,20%的患者的生存期均超过了两年,还有10%的患者至今仍在持续用药,无进展生存期达28-38个月之多。刘强教授表示,对于晚期三阴性乳腺癌的患者而言,这一结果可谓惊人。而在数据的背后,不少患者的“重获新生”更令人印象深刻。刘强教授回忆了一次与死神争夺患者生命的经历:“2018年的一位肺和胸壁多发转移患者来就诊时状况非常差,对之前的三线化疗均原发耐药,她当时非常悲观,觉得2018年肯定过不去了,但是经过治疗后肿瘤得到了很好的控制,至今都没有进展,现在依然愉快健康的活着,前不久还从外面旅游回来。”资料显示,该研究是全球首次报道三阴性乳腺癌中的免疫与抗血管生成联合治疗。在看到确切的获益后,宋尔卫院士、刘强教授与解放军总医院第五医学中心江泽飞教授紧接着开展了一项大型III期临床研究,进一步评估卡瑞利珠单抗联合白蛋白紫杉醇、阿帕替尼一线治疗晚期三阴性乳腺癌的疗效,目前正在入组中。不仅是临床试验,刘强教授在日常的临床治疗中已经以抗血管生成联合卡瑞利珠单抗为基础,设计了多种组合方案,对不少晚期三阴性患者进行了个体化的精准治疗,有联合化疗或抗雄激素受体拮抗剂的,也有联合PARP抑制剂的。其中,一部分患者获得完全缓解(临床影像上肿瘤完全消失),不少是脑转移、肺转移和肝转移这样严重的内脏转移,好几例脑转移患者实现了一年以上的无进展生存,“这在过去不可想象。”在2021年1月举行的日本京都国际乳腺癌会议上,刘强教授应邀在线上与各国专家分享了这一结果,令参会的欧美和亚洲专家大为赞叹,国际知名学者Hope Rugo教授表现出很大兴趣,并与刘强教授仔细讨论类似的方案能否在美国应用。如何更进一步?晚期三阴乳腺癌对以该联合方案为基础的治疗有效率虽可高达40-60%,但不可否认的是,仍有很多患者无法获益于免疫治疗,如何进一步提升患者疗效或更精准地识别获益人群?在刘强教授看来,找到合适的生物标志物,明确三阴性乳腺癌中免疫联合抗血管治疗的适用人群是关键。目前研究发现与PD-1/PD-L1疗效相关性较大的生物标志物(Biomarkers)主要包括PD-L1表达、肿瘤突变负荷(TMB)、微卫星不稳定性(MSI)和肿瘤浸润淋巴细胞等。然而,不同的联合方案的预测性标志物是不同的。对此,刘强教授团队开展了II期临床研究获益的分子标志物相关分析,发现PD-L1阳性和阴性患者在免疫联合抗血管治疗中都有获益,因此PD-L1表达阳性与否不能作为该联合方案的疗效预测指标。同时还发现,肿瘤组织中的肿瘤浸润淋巴细胞数量、治疗后CD8阳性T细胞的增加幅度,以及血液里部分细胞因子的变化,可预测该联合治疗获益人群。以上发现最近发表在Breast Cancer Research And Treatment(BCRT)杂志上,但其有效性还有待正在进行的III期临床研究来验证。刘强教授还表示,对于晚期三阴乳腺癌,免疫治疗的应用越早效果越好。此外,及早识别出术后复发转移风险高的早期三阴乳腺癌人群,给予恰当的强化治疗,对于提高早期三阴乳腺癌治愈率非常关键。刘强教授团队设计了一项临床试验,通过监测血液里的循环肿瘤DNA,精准预测早期三阴性乳腺癌患者的复发风险,筛选出高危复发风险人群,给予标准治疗或强化的免疫治疗,以证实联合免疫治疗是否能够提高其治愈率,目前这个多中心临床研究正在入组中。用专业照亮前方谈到三阴性乳腺癌免疫治疗,刘强教授指出还有许多问题悬而未决,未来的发展方向是新的免疫治疗靶点药物开发、与其他药物的最佳联合方案及寻找精准有效的适用人群。进一步了解肿瘤与人体免疫系统之间的相互作用,才有助于探索更加有效的免疫治疗方案。而这需要临床医生、基础与临床研究者、大数据/AI等行业的科学家和药企共同努力,”“临床医生的最大成就是把患者从死亡边缘拉回,这种成就不仅要求医生有先进的救治理念和技术,还要依赖于新的治疗药物开发,国内的创新药企近几年不断提升创新和质量水平,研发出真正有效的原研抗肿瘤药物,为我国患者提供更长生存和更好的生活质量。”刘强教授说。
刘强 主任医师 中山大学孙逸仙纪念医院 乳腺肿瘤中心4349人已读





